Нейродегенератив авырулар(NDD) баш мие яки арка миендәге билгеле бер зәгыйфь нейрон популяцияләренең прогрессив яки даими югалуы белән характерлана. NDD классификациясе төрле критерийларга нигезләнергә мөмкин, шул исәптән нейродегенерациянең анатомик таралышы (мәсәлән, экстрапирамидаль бозылулар, фронтотемпораль дегенерация яки спиносеребелляр атаксияләр), беренчел молекуляр аномалияләр (амилоид-β, прионнар, тау яки α-синуклеин кебек) яки төп клиник билгеләргә (мәсәлән, Паркинсон авыруы, амиотрофик латераль склероз һәм деменция). Классификация һәм симптомнарның бу аермаларына карамастан, Паркинсон авыруы (PD), Амиотрофик латераль склероз (ALS) һәм Альцгеймер авыруы (AD) кебек бозылулар нейрон дисфункциясенә һәм ахыр чиктә күзәнәк үлеменә китерә торган уртак төп процессларны уртаклаша.
Дөнья күләмендә миллионлаган кеше NDD'лардан интегә, шуңа күрә Бөтендөнья сәламәтлек саклау оешмасы 2040 елга бу авырулар үсеш алган илләрдә үлемнең икенче төп сәбәбе булачак дип фаразлый. Аерым авырулар белән бәйле симптомнарны җиңеләйтү һәм контрольдә тоту өчен төрле дәвалау ысуллары булса да, бу авыруларның үсешен акрынайту яки дәвалау өчен нәтиҗәле ысуллар әлегә ачык түгел. Соңгы тикшеренүләр дәвалау парадигмаларының гади симптомнарны дәвалаудан күзәнәкләрне саклау механизмнарын куллануга күчүен күрсәтә, бу аларның хәленең начарлануын булдырмас өчен кулланыла. Күп санлы дәлилләр оксидатив стресс һәм ялкынсынуның нейродегенерациядә төп роль уйнавын күрсәтә, бу механизмнарны күзәнәкләрне саклау өчен мөһим максатлар итеп куя. Соңгы елларда фундаменталь һәм клиник тикшеренүләр гипербарик кислород терапиясенең (HBOT) нейродегенератив авыруларны дәвалаудагы потенциалын ачты.
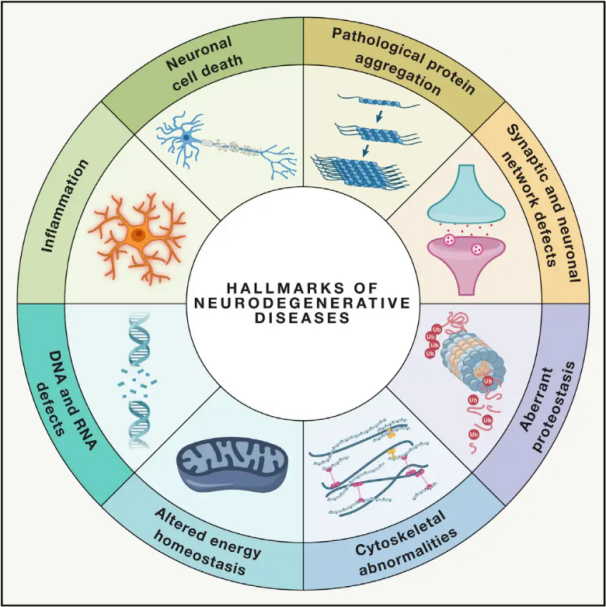
Гипербарик кислород терапиясен (ГБОТ) аңлау
HBOT гадәттә басымны 1 абсолют атмосферадан (ATA) югарыракка кадәр - диңгез дәрәҗәсендәге басымга - 90-120 минут дәвамында арттыруны үз эченә ала, еш кына дәвалана торган конкрет хәлгә карап берничә сеанс таләп ителә. Һава басымының артуы күзәнәкләргә кислород китерүне яхшырта, бу үз чиратында күзәнәкләрнең үрчүен стимуллаштыра һәм билгеле бер үсеш факторлары ярдәмендә дәвалау процессларын көчәйтә.
Башта HBOT куллану Бойл-Марриотт законына нигезләнгән, ул газ күбекләренең басымга бәйле кимүен, шулай ук тукымаларда югары кислород дәрәҗәсе файдасын күрсәтә. HBOT тарафыннан барлыкка килгән гипероксик халәттән файда күрүе билгеле булган төрле патологияләр бар, шул исәптән некротик тукымаларны, радиация җәрәхәтләрен, травмаларны, пешүләрне, компартмент синдромын һәм газ гангренасын, шул исәптән Су асты һәм гипербарик медицина җәмгыяте тарафыннан күрсәтелгән башкаларны да. Шунысы игътибарга лаек, HBOT шулай ук төрле ялкынсыну яки йогышлы авырулар модельләрендә, мәсәлән, колит һәм сепсиста өстәмә дәвалау буларак нәтиҗәлелеген күрсәтте. Ялкынсынуга каршы һәм оксидлашу механизмнарын исәпкә алып, HBOT нейродегенератив авыруларны дәвалау ысулы буларак зур потенциал тәкъдим итә.
Нейродегенератив авыруларда гипербарик кислород терапиясенең клиникка кадәрге тикшеренүләре: 3×Tg тычкан моделеннән алынган мәгълүматлар
Күренекле тикшеренүләрнең берсеАльцгеймер авыруының (АЧ) 3×Tg тычкан моделенә юнәлтелгән, ул HBOTның когнитив җитешсезлекләрне бетерүдәге терапевтик потенциалын күрсәтте. Тикшеренүдә 17 айлык 3×Tg ир тычканнары, ә контроль төркемдә хезмәт итүче 14 айлык C57BL/6 ир тычканнары катнашты. Тикшеренү HBOTның когнитив функцияне яхшыртуын гына түгел, ә ялкынсынуны, бляшка йөкләнешен һәм Тау фосфорлашуын да сизелерлек киметүен күрсәтте - бу АЧ патологиясе белән бәйле мөһим процесс.
HBOT-ның саклагыч йогынтысы нейроялкынсынуның кимүе белән бәйле дип табылды. Моны микроглиаль пролиферация, астроглиоз һәм ялкынсынуга каршы цитокиннар бүленеше кимүе күрсәтә. Бу ачышлар HBOT-ның когнитив эшчәнлекне яхшыртудагы һәм шул ук вакытта Альцгеймер авыруы белән бәйле нейроялкынсыну процессларын киметүдәге икеләтә ролен ассызыклый.
Клиникага кадәрге башка модельдә HBOTның нейрон функциясенә һәм хәрәкәт мөмкинлекләренә саклау механизмнарын бәяләү өчен 1-метил-4-фенил-1,2,3,6-тетрагидропиридин (MPTP) тычканнары кулланылган. Нәтиҗәләр HBOTның бу тычканнарда хәрәкәт активлыгын һәм тотыну көчен арттыруга өлеш кертүен күрсәтте, бу митохондриаль биогенез сигнализациясенең артуы белән бәйле, аеруча SIRT-1, PGC-1α һәм TFAM активлаштыру аша. Бу HBOTның нейропротектор йогынтысында митохондриаль функциянең мөһим ролен күрсәтә.
Нейродегенератив авыруларда HBOT механизмнары
NDDлар өчен HBOT куллануның төп принцибы кислород белән тәэмин итүнең кимүе һәм нейродегенератив үзгәрешләргә бирешүчәнлек арасындагы бәйләнештә ята. Гипоксия белән индукцияләнә торган 1 нче фактор (HIF-1) түбән кислород киеренкелегенә күзәнәк адаптациясен тәэмин итүче транскрипция факторы буларак үзәк роль уйный һәм төрле NDDларда, шул исәптән AD, Паркинсон авыруы, Хантингтон авыруы һәм ALSда катнаша, аны мөһим дару максаты итеп билгели.
Яшь күп нейродегенератив бозылулар өчен мөһим куркыныч факторы булганлыктан, HBOTның картаю нейробиологиясенә йогынтысын тикшерү бик мөһим. Тикшеренүләр күрсәткәнчә, HBOT сәламәт өлкән яшьтәге кешеләрдә яшькә бәйле когнитив җитешсезлекләрне яхшырта ала.Моннан тыш, хәтер бозылулары сизелерлек булган өлкән яшьтәге пациентларда HBOT тәэсиреннән соң когнитив яхшырулар һәм церебраль кан әйләнеше арту күзәтелде.
1. HBOTның ялкынсынуга һәм оксидатив стресска йогынтысы
HBOT баш миенең авыр дисфункциясе булган пациентларда нейроялкынсынуны киметү сәләтен күрсәтте. Ул ялкынсынуга каршы цитокиннарны (IL-1β, IL-12, TNFα һәм IFNγ кебек) киметү, ә ялкынсынуга каршы цитокиннарны (IL-10 кебек) көчәйтү сәләтенә ия. Кайбер тикшеренүчеләр HBOT тарафыннан барлыкка килгән реактив кислород төрләре (ROS) терапиянең берничә файдалы эффектын арадашчылык итә дип фаразлыйлар. Нәтиҗәдә, аның басымга бәйле күбекләрне киметү тәэсиреннән һәм тукымаларның югары кислород белән туендырылуына ирешүеннән тыш, HBOT белән бәйле уңай нәтиҗәләр өлешчә җитештерелгән ROSның физиологик рольләренә бәйле.
2. HBOTның апоптозга һәм нейропротекциягә йогынтысы
Тикшеренүләр күрсәткәнчә, HBOT гиппокампаль фосфорлашуны p38 митоген белән активлаштырылган протеин киназының (MAPK) гиппокампаль фосфорлашуын киметә ала, шуның белән танып белүне яхшырта һәм гиппокампаль зыянны киметә. Аерым HBOT та, гинкго билоба экстракты белән берлектә дә Bax экспрессиясен һәм каспаза-9/3 активлыгын киметә, нәтиҗәдә aβ25-35 белән индукцияләнгән кимерүчеләр модельләрендә апоптоз тизлеге кимүе ачыкланган. Моннан тыш, башка бер тикшеренү HBOTның баш мие ишемиясенә каршы толерантлыкны китереп чыгаруын күрсәтте, механизмнар SIRT1 экспрессиясенең артуын, B-күзәнәкле лимфома 2 (Bcl-2) дәрәҗәсенең артуын һәм актив каспаза-3 кимүен үз эченә ала, бу HBOTның нейропротектор һәм апоптозга каршы үзлекләрен ассызыклый.
3. HBOTның кан әйләнешенә йогынтысы һәмНейрогенез
HBOT белән зарарланган кешеләргә тәэсир итү баш сөяге кан тамырлары системасына күп төрле йогынты ясый, шул исәптән кан-баш мие барьеры үткәрүчәнлеген арттыра, ангиогенезны стимуллаштыра һәм шешенүне киметә. Тукымаларга кислород белән тәэмин итүне арттырудан тыш, HBOTкан тамырлары формалашуын стимуллаштыракан тамырлары эндотелиаль үсеш факторы кебек транскрипция факторларын активлаштыру һәм нерв күзәнәкләренең пролиферациясен стимуллаштыру юлы белән.
4. HBOT-ның эпигенетик йогынтысы
Тикшеренүләр күрсәткәнчә, кеше микроваскуляр эндотелиаль күзәнәкләренә (HMEC-1) гипербарик кислород тәэсир итү 8101 генны, шул исәптән югарырак һәм түбәнрәк экспрессияләрне дә, сизелерлек дәрәҗәдә көйли, бу антиоксидант җавап юллары белән бәйле ген экспрессиясенең артуын күрсәтә.
Йомгак
HBOT куллану вакыт узу белән зур уңышларга иреште, клиник практикада аның кулланылышын, ышанычлылыгын һәм куркынычсызлыгын раслады. HBOT NDDларны дәвалау өчен махсус ысул буларак өйрәнелсә дә һәм кайбер тикшеренүләр үткәрелсә дә, бу авыруларны дәвалауда HBOT практикасын стандартлаштыру өчен җитди тикшеренүләргә ихтыяҗ кала. Оптималь дәвалау ешлыгын билгеләү һәм пациентлар өчен файдалы йогынты дәрәҗәсен бәяләү өчен алга таба тикшеренүләр бик мөһим.
Кыскасы, гипербарик кислород һәм нейродегенератив авырулар кисешүе терапевтик мөмкинлекләрдә өметле чик күрсәтә, бу клиник шартларда өйрәнүне һәм валидацияне дәвам итүне таләп итә.
Бастырылган вакыты: 2025 елның 16 мае

